Bei Gehirnerkrankungen wie Alzheimer, Parkinson-Syndrom, Epilepsie und depressiven Störungen gibt es noch zahlreiche unbekannte Elemente, die uns diese Krankheiten noch nicht in ihrer Ganzheit verstehen lassen. Der Fonds Brain Diseases wurde dazu geschaffen, Antworten auf diese Fragen zu finden.
Der Fonds Brain Diseases unterstützt nicht-klinische Grundlagenforschung an der Universität Zürich in Form von Nachwuchsförderung. Die Mittel des Fonds Brain Diseases setzt die UZH Foundation für jährliche Anerkennungspreise junger Wissenschaftlerinnen und Wissenschaftler in Form des UZH Award for Research in Brain Diseases ein, der 2006 erstmalig vergeben worden ist. Für die Vergabe der Mittel ist ein Förderbeirat zuständig.
Sie doktorieren und suchen nach einer Unterstützungsmöglichkeit, die Ihrer Forschung auf dem Gebiet von Gehirnerkrankungen Auftrieb gibt? Bewerben Sie sich für den Brain Diseases Award und stellen Sie sich einer hochkarätigen Jury, die Ihre Forschungsergebnisse professionell bewertet. Unter allen Einreichungen werden jährlich Preise à 10 000 Franken für besonders bemerkenswerte Forschungsleistungen vergeben. Bitte entnehmen Sie diesem Dokument die Teilnahmebedingungen (in Englisch). Senden Sie Ihre vollständigen Bewerbungsunterlagen jeweils per 30. April in einem PDF-Dokument an Prof. Dr. Amedeo Caflisch.
Teilnahmebedingungen Brain Diseases Award (English)
Der Förderbeirat besteht aus folgenden Mitgliedern:
Prof. Dr. Amedeo Caflisch, Direktor Biochemisches Institut UZH, Vorsitz
Prof. Dr. Sebastian Jessberger, Direktor Institut für Hirnforschung UZH
Prof. Dr. Ben Schuler, Biochemisches Institut UZH

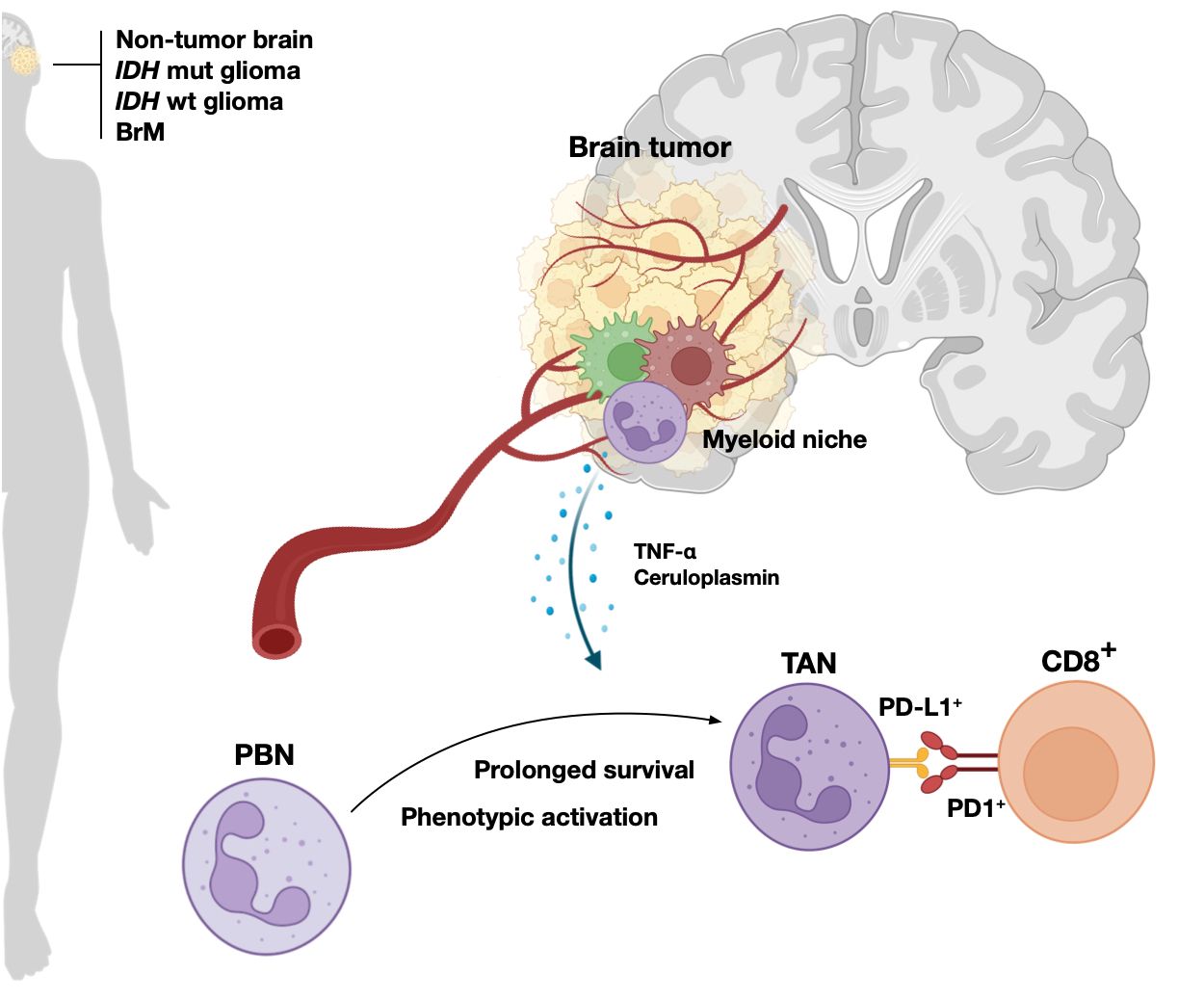
Tumor-assoziierte neutrophile Granulozyten (TANs) kommen in hochgradigen Gliomen und Hirnmetastasen beim Menschen sehr häufig vor, doch ist unklar, welche Rolle sie bei diesen Tumoren spielen. Wir konnten zeigen, dass TANs im Vergleich zu zirkulierenden Neutrophilen eine verlängerte Lebensspanne und einen immunsuppressiven Phänotyp durch die Expression von PD-L1 aufweisen. Darüber hinaus ko-lokalisieren PD-L1+ TANs mit PD1+ CD8+ T-Zellen, um eine effektive T-Zell-Hemmung zu bewirken. Wir haben herausgefunden, dass TNF-α und Ceruloplasmin, die von myeloischen Zellen in der Tumormikroumgebung (TME) produziert werden, diesen immunsuppressiven TAN-Phänotyp hervorrufen. Diese Erkenntnisse helfen, neue therapeutische Ziele zu finden, um das TME des Gehirns weniger immunsuppressiv und empfänglicher für eine Immuntherapie zu machen.

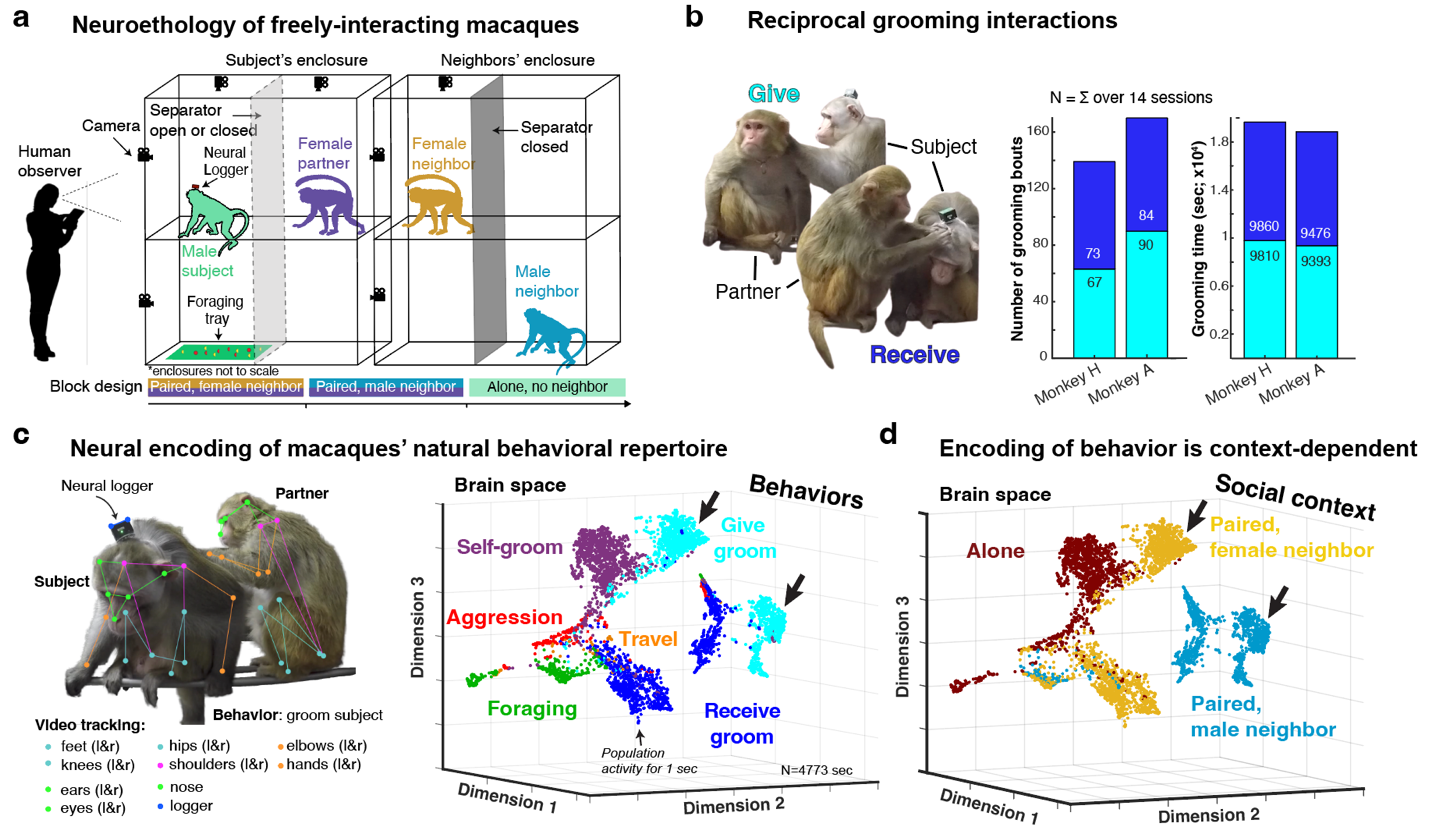
Soziale Interaktion ist entscheidend für die menschliche Gesundheit. Schlechte soziale Beziehungen werden unter anderem mit einem erhöhten Risiko für Herzkrankheiten, Schlaganfall, Depression und Demenz in Verbindung gebracht. Aus praktischen Gründen beschränken sich neurobiologische Untersuchungen der Sozialität von Primaten, einschließlich des Menschen, auf kontrollierte, computergesteuerte Aufgaben in sehr künstlichen Umgebungen. Trotz der Nützlichkeit dieses Ansatzes werden die natürlichen sozialen Verhaltensweisen vernachlässigt, für die Primatengehirne entwickelt wurden. Im Rahmen meiner Dissertation führte ich Ableitungen von Einzeleinheiten im temporalen und präfrontalen Kortex von sich frei bewegenden, sozial interagierenden Makaken durch. Ich fand eine hochgradig verteilte neuronale Aufzeichnung sozialer Dynamiken, von der Identität benachbarter Affen über soziale Unterstützung bei aggressiven Begegnungen bis hin zur Gegenseitigkeit in starken, stabilen Beziehungen - potenzielle neuronale Substrate, die den sozialen Bindungen zugrunde liegen, die das Überleben und den Fortpflanzungserfolg bei Primaten, einschließlich des Menschen, bestimmen.

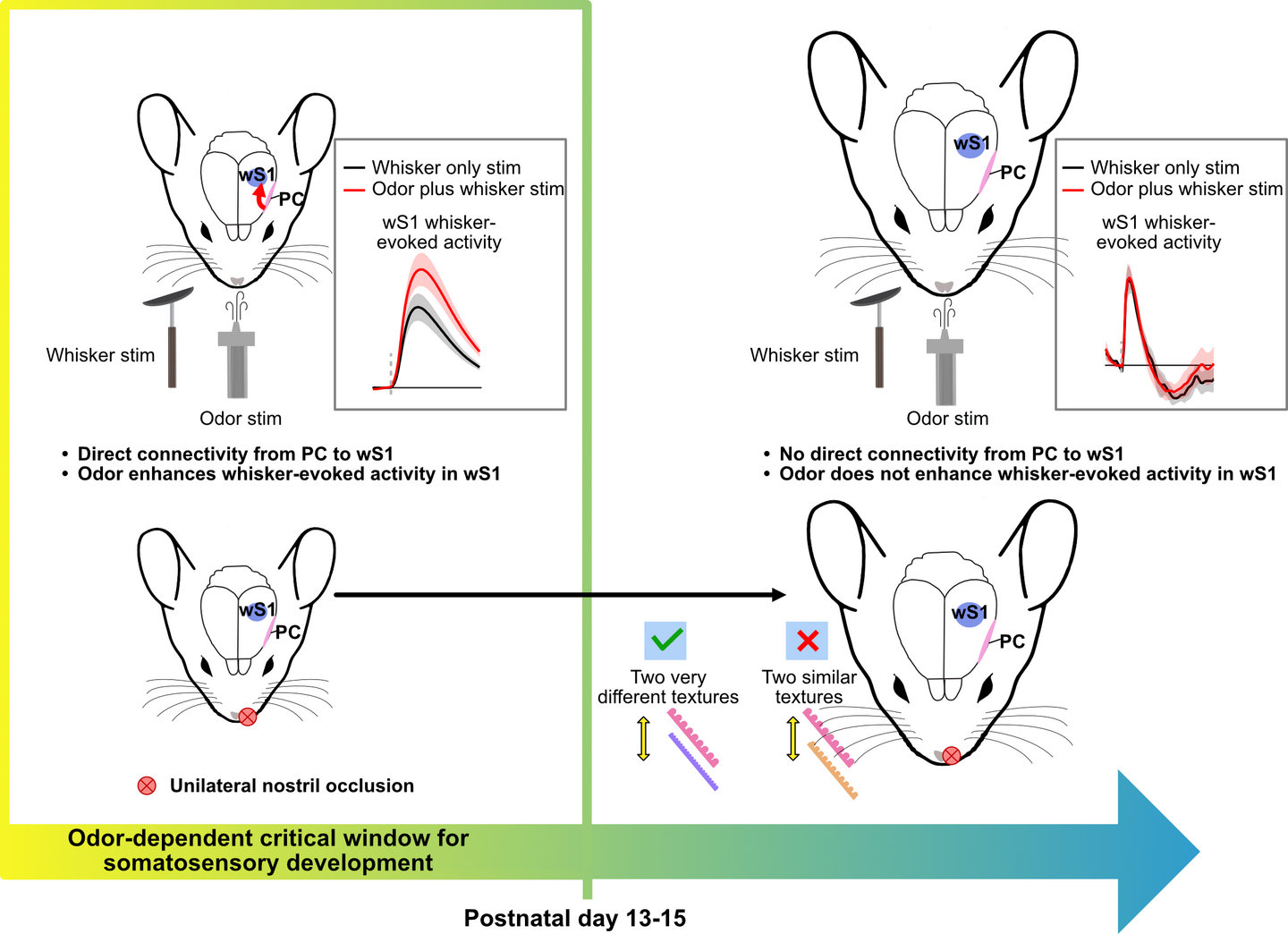
Die Mechanismen, die die Entwicklung und Integration der Sinnessysteme vermitteln, sind noch nicht vollständig geklärt. Wir untersuchten die Entwicklung des Geruchssystems, des evolutionär ältesten und frühesten funktionalen Sinnes, in Bezug auf die Somatosensorik. Wir konnten zeigen, dass sich Geruchsinformationen bei Mäusen in einer frühen postnatalen Phase, noch vor der Entwicklung anderer Sinne, über ein großes kortikales Gebiet, einschließlich des somatosensorischen Kortex (S1), ausbreiten. Diese geruchsvermittelte Erregung verstärkte bei Neugeborenen die durch Schnurrhaare hervorgerufene Aktivität in S1 und ging später in der postnatalen Entwicklung verloren. Geruchsdeprivation während der frühen Entwicklung beeinträchtigte die Somatosensibilität im späteren Leben, was auf die Existenz eines Entwicklungsfensters hindeutet, in dem der Geruchssinn die Entwicklung der somatosensorischen Verarbeitung beeinflusst. Diese Ergebnisse sind entscheidend für das Verständnis, wie sensorische Defizite die Gehirnreifung beim Menschen beeinflussen.
Mit Blick auf die bisher vergebenen Mittel lässt sich eine erfreuliche Besonderheit feststellen: Mehr als 20 der 30 Preise für bahnbrechende Ergebnisse in der Gehirnforschung wurden an Doktorandinnen verliehen. Der Brain Diseases Award zeichnet somit nicht nur grosses Innovationspotenzial aus, er fördert gleichzeitig auch Frauen in der Wissenschaft.
2023 Daniel Gonzalez-Bohorquez, Universität Zürich
Rolle der de-novo-Lipogenese bei der kortikalen Entwicklung und intellektuellen Behinderungen
2023 Manuela Pérez Berlanga, Universität Zürich
Verlust der TDP-43-Oligomerisierung oder RNA-Bindung führt zu unterschiedlichen Aggregationsmustern
2023 Yi Xiao Jiang, UCLA
Amyloidfibrillen bei FTLD-TDP bestehen aus TMEM106B und nicht aus TDP-43
2022 Sydney E. Cason, University of Pennsylvania
Sequential dynein effectors regulate axonal autophagosome motility in a maturation-dependent pathway
2022 Fadi Jacob, Johns Hopkins
A Patient-Derived Glioblastoma Organoid Model and Biobank Recapitulates Inter- and Intra-tumoral Heterogeneity.
2022 Lyle Kingsbury, UCLA
Correlated Neural Activity and Encoding of Behavior across Brains of Socially Interacting Animals
2021 Ekaterina Friebel, UZH
Single-Cell Mapping of Human Brain Cancer Reveals Tumor-Specifiv Instruction of Tissue-Invading Leukocytes
2021 Dasha Nelidova, University of Basel
Restoring light sensitivity using tunable near-infrared sensors
2021 David Tingley, NYU Neuroscience Institute
Routing of Hippocampal Ripples to Subcortical Structures via the Lateral Septum
2020 Claire Gizowski, UC San Francisco
Interplay between peripheral signals, behaviour and the central clock
2020 Sofie Ährlund-Richter, Karolinska Institute
On the Neuronal Correlates of Cognition: Cell-type specific Circuitry and Function of the Prefrontal Cortex
2020 Xuyu Qian, Harvard University
Modeling Human Brain Development and Disorders Using HiPSC-derived Organoids
2019 Sara Bottes, UZH
Live imaging of neurogenesis in the adult mouse hippocampus.
2018 Gioele La Manno, Karolinska Institute, Stockholm
RNA velocity in single cells.
2017 Tobias Wauer, University of Cambridge
Structure of the human Parkin ligase domain in an autoinhibited state.
2016 Lisa Traunmüller, University of Basel
Control of neuronal synapse specification by a highly dedicated alternative splicing program.
2015 Anne Maass, University of Magdeburg
Vascular hippocampal plasticity after aerobic exercise in older adults.
2014 Katharina Gapp, UZH
Implication of sperm RNAs in transgenerational inheritance of the effects of early trauma in mice.
2014 Marc Aurel Busche, TU München
Clusters of hyperactive neurons near amyloid plaques in a mouse model of Alzheimer's disease.
2013 Sandra Giovanoli, ETH Zurich
Stress in puberty unmasks latent neuropathological consequences of prenatal immune activation in mice.
2012 Amelie Ebke, LMU München
Novel γ-secretase snzyme modulators directly target presenilin protein.
2011 Stéphanie Vuillermot, ETH Zurich
The recombinant amyloid-beta peptide Abeta1-42 aggregates faster and is more neurotoxic than
synthetic Abeta1-42.
2010 Andreas Vitalis, Washington University in St. Louis
Quantitative characterization of intrinsic disorder in polyglutamine: insights from analysis based on
polymer theories.
2010 Verena Finder, ETH Zürich
The recombinant amyloid-beta peptide Abeta1-42 aggregates faster and is more neurotoxic than
synthetic Abeta1-42.
2009 Susanne Schneider, University of Lübeck
Mutations in the THAP1 (DYT6) gene- a cause of generalized dystonia with prominent spasmodic dysphonia.
2008 Carsten Sachse, University of Jena
Paired β-sheet structure of an Aβ(1-40) amyloid fibril revealed by electron microscopy
2008 Anat Frydman-Marom, University of Tel Aviv
Cognitive performance recovery of Alzheimer's disease model mice by modulating early soluble
amyloid assemblies.
2007 Eline Vrieseling, University of Basel
Target-induced transcriptional control of dendritic patterning and connectivity in motor neurons by
the ETS gene Pea3.
2007 Marlen Knobloch, UZH
Intracellular Aβ and cognitive deficits precede β-amyloid depositiobloch UZH'Intracellular Aβ and cognitive deficits precede β-amyloid depositiobloch UZH'Intracellular Aβ and cognitive deficits precede β-amyloid deposition in transgenic arcAβ mice.
2006 Mathias Heikenwälder, UZH
Chronic lymphocytic inflammation specifies the organ tropism of prions.
